在经典化学理论中,极性指一根共价键或一个共价分子中电荷分布的不均匀性。如果电荷分布得不均匀,则称该键或分子为极性;如果电荷分布得均匀,则称为非极性。
由于电荷概念其实在现代物理中是一个未解构内涵的概念,因此用“电荷分布不均匀”来解说分子的极性与非极性,是在用一个不可知概念来解说一种化学现象,这同样也不是科学作风。
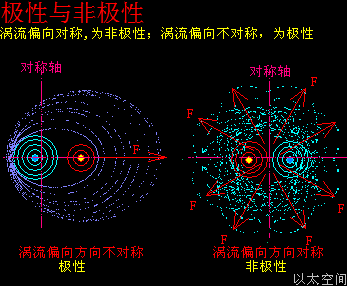
而通过共价键重新付予其内涵,及前面“电荷本质”小节中电荷是以太涡流的力场梯度分布的内涵解构,就可以知道分子极性与非极性的化学属性,源于分子次生以太旋涡的涡流偏向:
若次生涡流偏向是对称的,分子就表现出非极性。
若次生涡流偏向是不对称的,分子就表现出极性。
一般来说,由偶数相同原子以太旋涡耦合而成的分子以太旋涡,通常是非极性分子,如双原子同元素气体分子,氧气O2、氢气H2、乙炔C2H2都是非极性分子。而奇数原子以太旋涡耦合而成的分子以太旋涡,是极性分子,如臭氧O3、一氧化碳CO。
由奇偶数不同原子以太旋涡耦合成分子,则须具体分子具体分析,极性与否是由不同原子以太旋涡间的耦合结构的对称性决定,比如水分子H2O是极性分子,说明其分子结构是不对称的,而二氧化碳CO2是非极性分子,说明其分子结构是对称的。微观的原子以太旋涡耦合结构的对称性与宏观的化学物质的极性现象是相互映称的,可以对应检验。